Amonia
| Amonia | |
|---|---|
 |
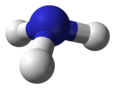 |
Azane | |
Jeneng liya Hydrogen nitride Trihydrogen nitride | |
| Identifikasi | |
| Nomor CAS | [7664-41-7] |
| PubChem | |
| Nomer EINECS | |
| KEGG | D02916 |
| MeSH | Ammonia |
| ChEBI | CHEBI:16134 |
| Nomer RTECS | BO0875000 |
| SMILES | N |
| InChI | 1/H3N/h1H3 |
| Réferènsi Baeilstein | 3587154 |
| Réferènsi Gmelin | 79 |
| 3DMet | B00004 |
| Sifat | |
| Rumus molekul | NH3 |
| Massa molar | 17.031 g/mol |
| Panampilan | Colourless gas with strong pungent odour |
| Densitas | 0.86 kg/m3 (1.013 bar at boiling point) 0.73 kg/m3 (1.013 bar at 15 °C) 681.9 kg/m3 at −33.3 °C (liquid)[1] 817 kg/m3 at -80 °C (transparent solid)[2] |
| Titik leleh |
−77.73 °C, 195 K, -108 °F |
| Titik umob |
−33.34 °C, 240 K, -28 °F |
| Kelarutan dalam air | 47% (0 °C) 31% (25 °C) 28% (50 °C)[3] |
| Kaasaman (pKa) | 32.5 (-33 °C),[4] 10.5 (DMSO) |
| Basicity (pKb) | 4.75 |
| Struktur | |
| Wangun molekul | Trigonal pyramid |
| Momen dipol | 1.42 D |
| Bahaya | |
| Klasifikasi EU | Toxic (T) Corrosive (C) Dangerous for the environment (N) |
| EU Index | 007-001-00-5 (anhydrous) 007-001-01-2 (solutions) |
| NFPA 704 | |
| Frasa-R | Cithakan:R10, Cithakan:R23, Cithakan:R34, Cithakan:R50 |
| Frasa-S | (S1/2), Cithakan:S9, S16, Cithakan:S26, Cithakan:S36/37/39, S45, Cithakan:S61 |
| Titik murub | flammable gas (see text) |
| Autoignition temperature |
651 °C |
| Explosive limits | 15–28% |
| U.S. Permissible exposure limit (PEL) |
50 ppm (25 ppm ACGIH- TLV; 35 ppm STEL) |
| Senyawa kagandhèng | |
| Kation liyané | Phosphine Arsine Stibine |
| nitrogen hydrides kagandhèng | Hydrazine Hydrazoic acid |
| Senyawa kagandhèng | Ammonium hydroxide |
| Kejaba ditélakaké suwaliké, data ing ndhuwur kanggo ing suhu lan tekanan standar (25°C, 100 kPa) | |
Amonia ya iku senyawa kimia kang duwé rumus NH3.[5] Lumrahé senyawa iki ana ing wujud gas kanthi ambu kang landhep lan kang khas (dikenal ambu amonia).[5] Amonia duwé fungsi kang wigati kanggo nutrisi ana ing bumi, amonia dhéwé ya iku senyawa kaustik kan bisa ngrusak kaséhatan.[5] Administrasi Keselamatan lan Keséhatan Pekerjaan Amérikah Sarékat mènèhi wates 15 menit kanggo kontak karo amonia ana ing gas berkonsentrasi 35 ppm volum, utawa 8 jam kanggo 25 ppm volum.[5] Kontak karo gas amonia kang konsentrasine dhuwur bisa nyebabake kerusakan ing paru-paru malah bisa nganti nyebabake mati.[5] Amonia ana ing AS diatur dadi gas kang ora gampang kobong nanging amonia isih dilebokaké ana ing golongan bahan mawa racun yèn kasedhot nalika ambegan, lan nalika ngangkud amonia kang cacahé punjul 3.500 galon (13,248 L) kudu dibarengi karo surat izin.[5] Amonia kang dipigunakaké kanggo komersial dijenengi amonia anhidrat.[5] Istilah iki nuduhaké ora mung amarga anané banyu ing bahan iku.[5] Amarga amonia umob ana ing suhu -33 °C, cuwèran amonia kudu disimpen ana ing tekanan dhuwur utawa temperatur cendhèk banget.[5] Perkara kang kaya mau, nanging kalor penguapane dhuwur banget nganti bisa ditangani karo tabung reaksi biyasa ana ing njeroné sungkup beluk.[5] "Amonia rumah" utawa amonium hidroksida ya iku larutan NH3 ing njero banyu.[5] Konsentrasi larutan iku diukur ana ing ékan baumé.[5] Produk larutan komersial amonia kang konsentrasiné dhuwur racaké duwé 26 derajat baumé (watarar 30 persèn saka boboté amonia ing 15.5 °C).[5]
Rujukan
[besut | besut sumber]- ↑ Yost, Don M. (2007). "Ammonia and Liquid Ammonia Solutions". Systematic Inorganic Chemistry. READ BOOKS. kc. 132. ISBN 1-4067-7302-6.
- ↑ Blum, Alexander (1975). "On crystalline character of transparent solid ammonia". Radiation Effects and Defects in Solids. 24 (4): 277. doi:10.1080/00337577508240819.
- ↑ Perry, Dale L.; Phillips, Sidney L. (1995). Handbook of inorganic compounds. CRC Press. kc. 17. ISBN 0-8493-8671-3.
{{cite book}}: CS1 maint: multiple names: authors list (link) - ↑ Perrin, D.D., Ionisation Constants of Inorganic Acids and Bases in Aqueous Solution; 2nd Ed., Pergamon Press: Oxford, 1982.
- ↑ a b c d e f g h i j k l m PubChem Substance Summary, last accessed May 7 2007
Pranala njaba
[besut | besut sumber]
| Artikel iki minangka artikel rintisan. Kowé bisa ngéwangi Wikipédia ngembangaké. |

