Réaksi kimia


Réaksi kimia inggih punika prosés alam ingkang asring ngasilaken éwahan Senyawa Kimia.[1] Sényawa utawi sényawa-sényawa wiwit ingkang gégayutan ing réaksi saged dipunsébapaken dados réaktan. Réaksi kimia dipunkaraktérisasikakén kaliyan Pérubahan kimiawi, lan badhé ngasilaken sétunggal utawi langkung produk ingkang gadhah titikan ingkang bèntén saking réaktan. Sécara klasik, réaksi kimia ngayutakén kaewahan pérgérakan Èlèktron ing pémbéntukan lan pémutusan ikatan kimia, manawi konsèp umum réaksi kimia ugi saged dipuntérapakè ing transformasi partikel-partikel elementer sami kaliyan reaksi nuklir. Reaksi-reaksi kimia ingkang panggènipun dipun-ginakaken sami ing sintesis kimia kanggé ngasilakné produk senyawa ingkang sampun dados ancasipun. Ing salébéting biokimia reaksi kimia dipunkatalisis kaliyan enzim mbéntuk lintasan métabolismé, ing sintesèis saha dekomposisi ingkang limrahipun botén kédadosan ing sèl
Séjarah
[besut | besut sumber]

Rèaksi kimia kados ta pangobong, férméntasi, lan rèduksi saking bijih dados logam sampun dipunmangértosi jaman rumiyèn.Téyori-téyori wiwit transformasi saking matérial-matérial punika dirémbakaké déning filsuf Yunani Kina, kadas Èlèmèn klasik saking Empedocles ingkang ngendika manawi substansi kèmawon kasusun saking èlèmèn dhasar inggih punika: Lati,toya, udara, lan [[bu.ing abad perètengahan, transformasi kimia dipunsinauni déning para alkemis. Sédaya nyobi, tuladhanipun, ngubah timbal dados émas, kaliyan ngèrèaksiakén timbal kaliyan campuran témbaga timbal kaliyan sulfur.[2] Produksi saking sényawa-sényawa kimia ingkang botén wonten kanthi alami ing donya, sampun lami para ilmuan, kados sintèsis saking asem sulfur lan asem nitrat saking alkemis Jābir ibn Hayyān. Prosès punika dipunlampahi kanthi cara béntérakèn minéral-minéral sulfat, saha nitrat, kados témbaga sulfat, alum lan kalium nitrat. Ing abad kaping 17, Johann Rudolph Glauber mroduksi asem klorida lan natrium sulfat kaliyan ngréaksiakén asem sulfat kaliyan natrium klorida. Wontén ananè parémbagan lead chamber process ing taun 1746 lan prosès Leblanc, pramila manawi wonten asem sulfat lan natrium karbonat ing jumlah ageng, mila rèaksi kimia saged dipunaplikasikakén ing indhustri. Tèknologi asem sulfat sampun majéng, pungkasaning saged ngasilaken prosès kontak ing taun 1880-an,[3] lan prosès Haber dipunembagagen ing taun 1909–1910 kanggé sintesis amonia.[4] Saking abad 16 peneliti kaya déné Jan Baptist van Helmont, Robert Boyle saha Isaac Newtonnyobi kanggé némtuakén téyori-téyori saking transformasi-transformasi kimia ingkang sampun dipuneksperimenaken ing Tèori plogiston dipuncetusaken ing taun 1667 déning Johann Joachim Becher. Téyori punika mempostulataken ananè èlèmèn kayadènè lati ingkang saged dipunwastani "plogiston", ing salébéting bandha-bandha ingkang sagét kabakar saha dipunuwalakén ngantas pangobong. Téyori punika dipunbuktiaken luput ing taun 1785 déning Antoine Lavoisier, ing pungkasan nyukani pangèrtosan ingkang lérés babagan pangobong.[5] Ing taun 1808, Joseph Louis Gay-Lussac mangertosi karakteristik gas sapunika sami. Adédasar ing téyori saking John Dalton, Joseph Proust saha ngerembakaken ukum perbandingan tetapingkang badhé dados konsèp wiwit saking stoikiometri saha persamaan reaksi.[6]
Saminipun
[besut | besut sumber]Persamaan rèaksi dipunginakakén kanggé rèaksi kimia. Sami rèaksi saking rumus kimia utawi rumus struktur saking rèaktan sisih kiwa lan produk ing sisih téngèn. Antawis produk lan rèaktan dipunpisahakén kaliyan pratitis(→) ingkang nunjukakè arah lan tipé rèaksi. Ujung saking pratanda kasébut nuduhaké rèaksi owah saking arah pundhi. Pratitis panah ganda (Cithakan:Eqm), ingkang gadhah kalih ujung tanda panah ingkang bènten arahipun, diginakakè ing rèaksi kéetimbangan. Saminipun kimia kédhahipun séimbang, jumbuh kaliyan stoikiometri, jumlah atom sabén unsur ing sisih kiwa kédhah sami kaliyan jumlah atom sabén unsur ing sisih téngén. Pényéimbangan punika dipunlampahi supadas nambah angka ing ngajéng molèkul senyawa (dipunlambangaken kaliyan A, B, C dan D dipundiagramaken skèma ing ngandap) kaliyan angka alit (a, b, c dan d) ing ngajengipun.[7]
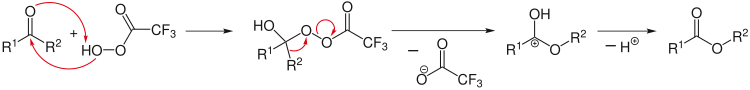
Rèaksi ingkang langkung rumit dipungambaraken kaliyan skèma réaksi, ancasipun kanggé mangertosi sényawa wiwit utawi pungkasan, utawi ugi nunjukakén fasé transisi. Pintén-pintén rèaksi kimia ugi saged dipuntambahakén sératan ing inggil tanda panah, tuladhanipu penambahan toya, béntèr, iluminasi, katalisasi, ugi pintén-pintén produk minor saged dipunpanggénakén ing ngandap panah.

Analisis rétrosintetik saged diginaakèn kanggé désain rèaksi sintèsis komplèks. Analisis dipunwiwiti saking produk, tuladhanipun mécah ikatan kimia ingkang kapilih dados reagen ènggal. Tanda panah mirunggan (⇒) diginakakén ing réaksi rètro.[8]
Rèaksi Èlèmèntèr
[besut | besut sumber]Rèaksi Èlèmèntèr inggih punika pemecahan prasaja lan asil saking rèaksi punika botén gadhah produk sampingan..[9] Kathah rèaksi ingkang kasilipun kapanggih inggih punika ngérémbag saking rèaksi Èlèmèntèr ingkang tuwuh kanthi paralèl tuwin runtut. Sebuah rèaksi Èlèmèntèr saking pintén-pintén.[10]
- Disoasi dari molekul AB menjadi fragmen A dan B
Ing reaksi bimolekular, 2 molekul badhé bertabreakan lan saling bereaksi. kasil reaksinipun dipunnamani sintesis kimia utawa reaksi adisi.
Kemungkinan reaksi ingkang sanès inggih punika péranganing sebuah molekul gantos ing sanèsipun. Reaksi jinis kados ta punika, tuladhané inggih punika reaksi redoks lan reaksi asem-basa. Ing reaksi redoks partikel ingkang gantos inggih punika èlèktron, nanging ing reaksi asem-basa ingkang gantos proton. Reaksi kados ta punika ugi dipunsebat kaliyan reaksi metatesis.
contohnya
Termodinamika
[besut | besut sumber]Reaksi kimia saged kapanggih déning ukum-ukum termodinamika. Reaksi saged kadadosan kaliyan piyambakipun manawi senyawa mau eksergonik utawi nguwalaken ènergi. Energi bébas ingkang dipunkasilaken reaksi punika kapérang saking 2 besaran termodinamika inggih punika entalpi lan entropi]]:[11]
- G: ènergi bébas, H: entalpi, T: suhu, S: entropi, Δ: perbedaan
Reaksi eksotermik kadadosan manawi ΔH gadhah aji négatif lan ènergi dipunuwalaken. Tuladhaipun reaksi eksotermik inggih punika presipitasi lan kawalikanipun, salebeting reaksi endotermik, benter dipunpendet saking lingkungan. Sapunika saged dipunlampahi kaliyan ningkataken entropi sistem. amargi kenaikan entropi bandinganipun lurus kaliyan ingkang boten kasunyatan, kathah reaksi eksotermik dipunlampahi ing suhu ingkang cendhèk. Owah-owahan témperatur punika saged ngewahi arah reaksi, kados ta tuladha ing reaksi Boudouard:
Reaksi antawis karbon dioksida lan karbon kanggé minangka karbon monoksida punika reaksi endotermik kaliyan suhu ing inggil 800 °C lan dados reaksi eksotermik mila suhunipun ing ngandap punika [12]
Reaksi ugi saged nglampahi saged ningali lan ugi saged dipunmangertosi kaliyan ènergi dalam ingkang nyebataken kauwalan ing entropi, volume, lan potensial kimia.[13]
- U: ènergi ing, S: entropi, p: tekanan, μ: po]tensial kimia, n: jumlah molekul, d: tanda ingkang tegesipun kaewahan alit
Pengelompokan Reaksi Kimia
[besut | besut sumber]Aneka warni reaksi-reaksi kimia lan pendekatan-pendekatanipun ingkang dipunlampahi ing pasinaon njalari kathah cara kanggé klasifikasiaken reaksi-reaksi mau, ingkang asring tumpang tindih. ing ngandap punika tuladha-tuladha klasifikasi reaksi kimia ingkang limrahipun dipun-ginakaken.
Sekawan reaksi dhasar
[besut | besut sumber]Sintesis
[besut | besut sumber]Ing reaksi kombinasi langsung utawi sintesis, kalih utawi langkung senyawa prasaja gegayutan minangka senyawa énggal ingkang langkung kompleks. Kalih reaktan utawi langkung ingkang bereaksi ngasilaken satunggal produk ugi punika salah satunggaling cara kanggé mangertosi manawi reaksi sintesis. Tuladha saking reaksi punika inggih punika gas hidrogen gegayutan kaliyan gas oksigèn ingkang kasilipun inggih punika toya.[14]
Tuladha sanès inggih punika gas nitrogen gegayutan kaliyan gas hidrogen badhé minangka amoniak, kaliyan sami reaksi:
Dekomposisisi
[besut | besut sumber]Reaksi dekomposisi utawi analisis inggih punika ingkang boten kasunyatan saking reaksi sintesis. Sebuah senyawa ingkang langkung kompleks badhé dipunpecah dados senyawa ingkang langkung prasaja.[14][15] Tuladhanipun inggih punika molekul toya ingkang dipunpecah dados gas oksigèn lan gas hidrogen, kaliyan sami reaksi:
Panggantosan tunggal
[besut | besut sumber]Ing reaksi penggantian tunggal utawi substitusi, sebuah unsur tunggal gantosaken unsur tunggal sanèsipun ing suatu senyawa. Tuladhanipun inggih punika logam natrium ingkang bereaksi kaliyan asem klorida badhé ngasilaken natrium klorida utawi uyah dapur, kaliyan persamaaan reaksi:
Pangertosan ganda
[besut | besut sumber]Ing reaksi pargantosan ganda, kalih senyawa punika gantos ion utawi ikatan kanggé minangka senyawa énggal ingkang bènten.[14] punika kadadosan ing wanci kation lan anion saking 2 senyawa ingkang bènten saling gantos panggènan, lan minangka kalih senyawa énggal.[15] Rumus umum saking reaksi punika inggih punika:
- AB + CD → AD + CB
Tuladha saking reaksi gantosan ganda inggih punika timbal(II) nitrat bereaksi kaliyan kalium iodida kanggé minangka timbal(II) iodida lan kalium nitrat, kaliyan sami reaksi:
- Pb(NO3)2 + 2 KI → PbI2 + 2 KNO3
Tuladha sanès inggih punika natrium klorida (uyah dapur) bereaksi kaliyan pérak nitrat minangka natrium nitrat lan pérak klorida, kaliyan persamaan reaksi:
Oksidasi dan reduksi
[besut | besut sumber]
Reduction
Oxidant + e– ⟶ Product
(Electrons gained; oxidation number decreases)
Oxidation
Reductant ⟶ Product + e–
(Electrons lost; oxidation number increases)
Reaksi redoks saged dipunpahami dados transfer èlèktron saking salah satunggaling senyawa (dipunsebat reduktor) ing senyawa sanèsipun (dipunsebat oksidator). Ing prosès punika, senyawa ingkang satunggal badhé teroksidasi lan senyawa sanèsipun badhé tereduksi, amargi punika mau redoks. Oksidasi piyambak dipunmangertosi dados kenaikan bilangan oksidasi, lan reduksi inggih punika penurunan bilangan oksidasi. ing praktekipun, transfer saking èlèktron punika badhé ngewahi wilangan oksidasinipun, nanging kathah reaksi ingkang dipunklasifikasiaken dados reaksi redoks manawi sajatosipun boten wonten èlèktron ingkang gantos (kados ta ingkang gayutaken ikatan kovalen).[16][17] Tuladha reaksi redoks inggih punika:
- 2 S2O32−(aq) + I2(aq) → S4O62−(aq) + 2 I−(aq)
- Yang mana I2 dipunreduksi dados I- lan S2O32- (anion tiosulfat) dipunoksidasi dados S4O62-.
Kangge mangertosi reaktan pundhi ingkang badhé dados agen pereduksi lan pundhi ingkang badhé dados agen teroksidasi saged dipunmangertosi saking keelektronegatifan unsur mau. Elemen ingkang gadhah aji keelektronegatifan ingkang cendhèk, kados ta kathah unsur logam, mila badhé gampil maringi èlèktron punika lan teroksidasi-unsur punika dados reduktor. sakwalike, kathah ion ngadahi bilangan oksidasi inggil, kados ta H2O2, MnO4-, CrO3, Cr2O72-, OsO4) saged pikoleh satu utawi langkung tambahan èlèktron, ngantos dipunsebat oksidator. Jumlah èlèktron ingkang dipunparingake utawi dipuntampi ing reaksi redoks saged dipunmangertosi saking konfigurasi elektronn unsur reaktanipun. Saben unsur badhé usaha kanggé dadosaken konfigurasi elektronipun sami kaliyan konfigurasi unsur gas mulia. Logam alkali lan halogen badhé maringi lan nampi satunggal èlèktron. Elemen gas alam piyambak sajatosipun boten aktif kanthi kimiawi.[18]
Salah satunggaling pérangan ingkang wigatos ing reaksi redoks inggih punika reaksi elektrokimia, ing pundhi èlèktron saking sumber listrik dipung reduktor. ingkang dados Reaksi punika wigati sadaya kanggé ndamel unsur-unsur kimia, kados ta klorin[19] utawi aluminium. Prosès reaksi redok boten kasunyatan ing pundhi dipun-ginakaken kanggé ngasilaken listrik ugi boten lan prinsip punika dipun-ginakaken ing baterai.
Reaksi asem-basa
[besut | besut sumber]Reaksi asem-basa inggih punika reaksi ingkang ndonoraken proton saking sebuah molekul asem ing molekul basa. Ing ngriki, asem gadhah peran dados donor proton lan basa gadhah peran dados akseptor proton.
- Reaksi asem basa, HA: asem, B: Basa, A–: basa konjugasi, HB+: asem konjugasi
Kasil saking transfer proton punika ya iku asem konjugasi lan basa konjugasi.[20] Reaksi kesetimbangan (bolak-balik) ugi wonten, lan amargi punika asem utawi basa lan asem utawi basa konjugasinipun punika wonten ing kesetimbanganipun. Reaksi kesetimbangan punika dipuntitiki kaliyan wontenipun konstanta diasosiasi asem lan basa (Ka dan Kb) saking saben substansinipun. Sebuah reaksi ingkang mliginipun saking reaksi asem-basa inggih punika netralisasi ing pundhi asem lan basa ing jumlah ingkang sami badhé minangka garam ingkang asifat nétral. Reaksi asem basa gadhah pinten-pinten dhéfinisi gumantung ing konsèp asem basa ingkang dipun-ginakaken. Pinten-pinten dhéfinisi ingkang paling umum inggih punika:
- Dhéfinisi Arrhenius: asem berdisosiasi ing toya ngelepasaken ion H3O+; basa berdisosiasi ing toya ngelepasaken ion OH-.
- Dhéfinisi Brønsted-Lowry: Asam inggih punika pendonor proton (H+) donors; basa inggih punika nampi (akseptor) proton. anglingkupi dhéfinisi Arrhenius
- Dhéfinisi Lewis: Asam inggih punika akseptor pasangan èlèktron; basa inggih punika pendonor pasangan èlèktron. Dhéfinisi punika anglingkupi dhéfinisi Brønsted-Lowry.
Presipitasi
[besut | besut sumber]
Presipitasi inggih punika prosès reaksi dumadi padatan (endapan) ing salebeting sebuah larutan dados kasil saking reaksi kimia. Presipitasi punika limrahipun dumadi ing konsèntrasi ion ingkang larut sampun gayuh wates kelarutan[21] lan kasilipun inggih punika minangka garam. Reaksi punika saged dipuncepetake manawi nambahaken agen presipitasi utawi ngirangi pelarutnipun. Reaksi presipitasi punika ingkang ngasilaken residu mikrokristalin lan prosès ingkang lambat badhé ngasilaken kristal tunggal. Kristal tunggal ugi saged pikoleh saking rekristalisasi saking garam mikrokristalin.[22]
Reaksi ing Zat Padat
[besut | besut sumber]Reaksi saged kadadosan ing antawisipun kalih bandha padat. nanging makaten, amargi tingkat difusi ing zat padat sanget cendhèk, mila reaksi kimia ingkang kalangsungaken dados sangat lambat. Reaksi saged dipuncepetake kaliyan cara ningkataken suhu pramila badhé mecah reaktan, pramila amba lumah kontak dados langkung ageng.[23]
Reaksi fotokimia
[besut | besut sumber]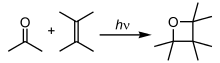
Ingreaksi fotokimia, atom lan molekul badhé nyerap ènergi (foton) saking cahya lan gayutaken ingeksitasi. Atom lan molekul punika lajeng saged ngelepasake ènergi kaliyan mecahake ikatan kimia, mila ngasilaken radikal. Reaksi ingkang kalebet ing reaksi fotokimia ing natawisipun reaksi hidrogen-oksigèn, polimerisasi radikal, reaksi berantai lan reaksi penataan ulang.[24] Kathah prosès-prosès ingkang wigati ngginakaken fotokimia. Tuladha ingkangg paling umum inggih punika fotosintesis, ing pundhi tuwuhan ngginakaken ènergi srengéngé kanggé ngubah karbon dioksida lan toya dados glukosa lan oksigèn dados kasil sampingan. Manungsa ngandalaken fotokimia ing pembentukan vitamin D, lan persepsi visual dipunkasilaken saking reaksi fotokimia ing rhodopsin.[25] Ing kunang-kunang, sebuah enzim ing abdomen ngkatalisasi reaksi ingkang ngasilaken bioluminesensi.[26] Kathah reaksi fotokimia, kados ta pembentukan ozon, kadadosan ing atmosfer bumi ingkang angliputi péranganing kimia atmosfer.
Katalisis
[besut | besut sumber]
Ing katalisis, reaksinipun boten kalangsungan kanthi spontan, nanging nglampahi substansi katiga ingkang dipunsebat kaliyan katalis. Boten kados ta reagen sanèsipun ingkang ndhèrèk ing reaksi kimia, katalis boten ndhèrèk sarta ing reaksi punika piyambak, nanging saged nghambat, matikan, utawi ngajuraken nglampahi prosès sékundhèr. Katalis saged dipun-ginakaken ing fase ingkang bènten-bènten (katalis heterogen) utawi ing fase ingkang sami (katalis homogen) dados reaktan. Fungsi katalis namung mempercepat reaksi-zat kimia ingkang ngelambataken reaksi dipunsebat kaliyan inhibitor.[27][28] Substansi yang meningkatkan aktivitas katalis dipunsebat promoter, lan substansi ingkang mematikan katalis dipunsebat racun katalis. Sebuah reaksi kimia ingkang sajatosipun boten kalangsungan amargi ènergi aktivasinipun langkung inggil, saged dados kalangsungan amargi wonten katalis punika. Katalis heterogen limrahipun padat lan wujud bubuk supados saged maksimalaken luas lumah ingkang bereaksi. Zat-zat ingkang wigati ing katalisis heterogen ing antawisipun logam-logam grup platinum lan logam transisi sanèsipun. Zat-zat punika limrahipun dipun-ginakaken ing hidrogenasi, pembentukan katalitik lan sintesis saking senyawa-senyawa kimia kados ta asem nitrat lan amonia. Asam inggih punika tuladha saking katalis homogen, punika ningkataken nukleofilitas saking karbonil. Kalangkungan saking katalis homogen inggih punika gampil kanggé dipuncampurake kaliyan reaktanipun, nanging kekiranganipun anggel anggene dipunpisahake saking produk pungkasanipun. Mekawi mekate, katalis heterogen langkung dipunpilih kathah prosès indhustri.[29]
Reaksi ingm kimia organik
[besut | besut sumber]Ing kimia organik, kathah reaksi ingkang saged kadadosan ingkang ngelibataken ikatan kovalen ing antawisipun atom karbon lan heteroatom sanèsipun kados ta oksigèn, nitrogen, utawi atom-atom halogen sanèsipun. Pinten-pinten reaksi ingkang langkung spesifik badhé njelentrehake ing ngandap punika.
Substitusi
[besut | besut sumber]Ing reaksi substitusi, sebuah gugus fungsi ing salebeting senyawa kimia dipungantosaken kaliyan gugus fungsi sanèsipun.[30] Reaksi punika saged dipunbentenaken ugi dados pinten-pinten subtipe inggih punika nukleofilik, substitusi elektrofilik, utawi substitusi radikal. direction = vertical | image1 = SN1 reaction mechanism.png|width1 = 300|image2 = SN2 reaction mechanism.png|width2 = 300| caption1 = SN1 mechanism| caption2 = SN2 mechanism Ing jinis ingkang kawiwitan, nukleofil, atom utawi molekul ingkang gadhah kalangkungan èlèktron pramila bermuatan négatif, badhé gantosaken atom sanèsipun utawi pérangan sanèsipun saking molekul "substrat". Pasangan èlèktron nukleofil badhé nyatu kaliyan substrat minangka ikatan énggal, nanging gugus lepas badhé nglepas sami kaliyan sebuah pasangan èlèktron. Nukleofil saged bermuatan nétral utawi positif, nanging substrat limrahipun bermuatan positif utawi nétral. Tuladhané nukleofil inggih punika ion hidroksida, alkoksida, amina, lan halida. Reaksi sairib punika limrahipun dipuntemuaken ing hidrokarbon alifatik lan boten dipuntemtuaken ing hidrokarbon aromatik. Hidrokarbon aromatik gadhah rapatan èlèktron inggal lan ngantos saged kalangsungan substitusi aromatik nukleofilik namung kaliyan gugus penarik èlèktron ingkang sangat kiat. Substitusi nukleofilik saged kalangsungan nglampahi 2 mekanisme, Reaksi SN1 lan SN2. Miturut namanipun, S cekakan saking substitusi, N singkatan dai nukleofilik, lan, angka nedahaken ordo kinetik reaksi, unimolekuler utawi bimolekuler.[31]
Reaksi SN1 kalangsungan ing kalih tahap. Tahap kawiwitan, gugus lepas badhé ngelepas lan minangka karbokation. Tahap punika badhé dipundereaken reaksi ingkang sanget rikat kaliyan nukleofil.[32] Ing mekanisme SN2, nukleofil badhé minangka tahap transisi kaliyan molekul ingkang uwal lan namung terlekang. Kalih mekanisme punika bènten-bènten ing kasil stereokimianipun. Reaksi SN1 ngasilaken adisi non-stereospesifik lan boten ngasilaken punjer chiral, nanging ing wujud isomer geometri (cis/trans). kawalikane, inversi Warden-punika ingkang dipunamati ing mekanisme SN2.[33] Substitusi elektrofilik punika kawalikan saking substitusi nukleofilik ing pundhi atom utawi molekul ingkang ngelepas, utawi elektrofilnipun, gadhah kerepetan èlèktron ingkang cendhèk ngantos bermuatan positif. Limrahipun elektrofil punika atom karbon saking gugus karbonil, karbokation utawi sulfur utawi kation nitronium. Reaksi punika kalangsungan ing hidrokarbon aromatik kemawon, pramila dipunsebat substitusi aromatik elektrofilik. Serangan elektrofil badhé nyiptaaken kompleks ingkang dipunsebat dados σ-compleks, sebuah fase transisi ing pundhi sistem aromatikipun ical. lajeng, gugus lepas (limrahipun proton), badhé kapisah lan sipat kearomatikipun balik. Alternatif sanès kanggé substitusi aromatik inggih punika substitusi alifatik elektrofilik. Substitusi punika sami kaliyan substitusi aromatik elektrofilik lan ugi gadhah kalih jinis utami inggih punika SE1 lan SE2[34]

Adisi lan eliminasi
[besut | besut sumber]Adisi lan pasanganipu eliminasi punika reaksi ingkang ngubah jumlah substituen ing atom karbon, lan minangka ikatan kovalen. Ikatan ganda lan tiga saged kaasilaken kaliyan mengeliminasi gugus lepas ingkang jumbuh. Kadasta substitusi nukleofilik, wonten pinten-pinten mekanisme reaksi ingkang kadadosan. Ing mekanisme E1, gugus lepas kalangkungan rumiyen ngelepas lan minangka karbokation. Salajengipun, minangka ikatan ganda kadadosan nglampahi eliminasi proton (deprotonasi). Dalam mekanisme E1cb, urutan pelepasan terbalik: proton dieliminasi terlebih dahulu. Dalam mekanisme punika ngelibataken suatu basa kedah wonten.[35] Reaksi ing eliminasi E1 utawi E1cb punika bersaing kaliyan substitusi SN1 amagi gadhah kaanan reaksi kondisi ingkang sami.[36]

Mekanisme E2 ugi mbetahaken basa. nanging, gantos panggènan basa lan eliminasi gugus uwal ingkang kalangsungan kanthi serentak lan boten ngasilaken zat antawisipun ionik. Benten kaliyan eliminasi E1, konfigurasi stereokimia ingkang bènten saged dipunkasilaken ing reaksi ingkang gadhah mekanisme E2 amargi basa badhé langkung memfavoritkan eleminasi proton ingkang wonten ing panggènan-anti kaliyan gugus uwal. Amargi kaanan lan reagen reaksi ingkang sami, eliminasi E2 punika bersaing dengan substitusi SN2.[37]

Kawalikan saking reaksi eliminasi inggih punika reaksi adisi. Ing reaksi adisi, ikatan rangkep kalih utawi rangkap tiga dipunubah dados ikatan rangkap tunggal. Sami kaliyan reaksi substitusi, wonten pinten-pinten jinis saking adisiingkang dipunbentenaken saking partikel ingkang ngadisi. Tuladhanipun, ing adisi elektrofilik hidrogen bromida, sebuah elektrofil (proton) badhé gantos ikatan rangkep ganda lan minangka karbokation, lajeng ngereaksi kaliyan nukleofil (bromin). Karbokation saged dumadi ing salah satunggaling ikatan rangkep gumantung saking gugus ingkang ngeleket ing pungkasan. Konfigurasi ingkang langkung trep saged dipunprediksiaken kaliyan aturan Markovnikov.[38] Aturan Markovnikov ngendikan: "Ing adisi heterolitik saking sebuah molekul polar ing alkena utawi alkuna, atom ingkang gadhah keelektronegatifan ingkang ageng, mila badhé kaiket ing atom karbon ingkang ngikat atom hidrogen ingkang langkung kedhik."[39]
Reaksi kimia organik sanèsipun
[besut | besut sumber]
Ing reaksi penataan ulang, kerangka karbon saking sebuah molekul dipunsusun malih pramila minangka isomer struktur saking molekul aslinipun. Reaksi punika kalebet reaksi sigmatropik kados ta penataan ulang Wagner-Meerwein, ing pundhi gugus hidrogen, alkil, utawi aril gantos-gantos panggènan saking suatu atom karbon ing atom karbon sanèsipun. Kathah reaksi penataan malih inggih punika pemutusan lan pambentukan ikatan karbon-karbon énggal. Tuladha sanès saking reaksi punika ya iku penataan ulang cope.[40]
Reaksi sanèsipun
[besut | besut sumber]- Isomerisasi, ing senyawa kimia nglampahi penataan malih struktur tanpa kauwahan ing komposisi atomipun
- Pembakaran, inggih punika sejinis reaksi redoks ingkang bahan-bahanipun ingkang saged kabakar gegayutan kaliyan unsur-unsur oksidator, limrahipun oksigèn, kange ngasilaken benter lan minangka produk ingkang teroksidasi. Istilah pangobong limrahipun dipun-ginakaken kanggé ngerujuk namung ing oksidasi skala ageng ing sadaya molekul. Oksidasi terkontrol namung ing satunggal gugus fungsi tunggal boten kalebet ing prosès pangobong.
- Disproporsionasi, kaliyan satunggal reaktan minangka kalih jinis produk ingkang bènten namung ing kaanan oksidasinipun.
- 2 Sn2+ → Sn + Sn4+
Kinetika kimia
[besut | besut sumber]Laju reaksi suatu reaksi kimia punika pengukuran konsèntrasi utawi tekanan zat-zat ingkang gegayutan ing reaksi kauwah ing kalampahan wekdal. Analisis laju reaksi punika wigati lan gadhah kathah mupangatipun, tuladhané ing tèhnik kimia lan kajian kesetimbangan kimia. Lajeng reaksi kanthi ndasar ngumantung ing:
- Konsentrasi reaktan, ingkang limrahipun ndamel reaksi kalampahan kaliyan langkung rikat manawi konsentrasinipun dipununggahake. punika amargi peningkatan pertumbukan atom per ékan wekdal,
- Jembar lumah ingkang kasedia kanggé reaktan kanggé saling berinteraksi, mliginipun reaktan padet ing sistem heterogen. Amba lumah ingkang ageng badhé ningkataken laju reaksi.
- Tekanan, kaliyan ningkataken tekanan, punika nurunaken volume antawis molekul pramila badhé ningkataken frekuensi tumbukan molekul.
- Energi aktivasi, ingkang dipundefinisiaken dados jumlah ènergi ingkang dipunbetahaken kanggé ndamel reaksi kawiwitan lan berjalan kanthi spontan. Energi aktivasi ingkang langkung inggil ngimplikasiaken manawi reaktan punika langkung mbetahaken kathah kanggé kawiwitan reaksi manawi reaksi ingkang berenergi aktivasi langkung cendhèk.
- Temperatur, ingkang ningkataken laju reaksi manawi dipunnaikaken, punika amargi témperatur ingkang inggil ningkaatken ènergi molekul, pramila ningkataken tumbukan antawis molekul per ékan wakdal.
- Panggènan utawi ketiadaan katalis. Katalis inggih punika zat ingkang ngubah lintasan (mekanisme) suatu reaksi lan badhé ningkataken laju reaksi kaliyan nurunaken ènergi aktivasi ingkang dipunbetahaken supados reaksi saged kalampahan. Katalis boten dipunkonsumsi utawi kaewah selama reaksi, pramila punika saged dipun-ginakaken malih.
- Kangge pinten-pinten reaksi, keberadaan radiasi èlèktromagnètik, utamanipun ultraviolet, dipunmbetahaken kanggé mutusaken ikatan ingkang dipunbetahaken supados reaksi saged wiwit. Utaminipun kadadosan ing reaksi ingkang ngelibataken radikal.
Laju reaksi gegayutan kaliyan konsèntrasi zat-zat ingkang gegayutan ing reaksi. Gegayutan punika dipuntemtuaken déning persamaan laju saben reaksi. Kedhah dipun-gantos manawi pinten-pinten reaksi gadhah kelajuan ingkang boten gumantung ing konsèntrasi reaksi. punika dipunsebat dados reaksi orde nol.
Reaksi biokimia
[besut | besut sumber]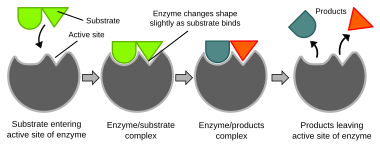
Reaksi biokimia ing limrahipun dipunkendaliaken déning enzim. Protein-protéin punika namung saged mengkatalis satunggal jinis reaksi ingkang spesifik, pramila reaksinipun punika saged dipunkontrol. Reaksi punika kalangsungan ing sisih aktif saking substrat. Reaksi katalisasi enzim punika gumantung ing kathah prekawis, ing antawisipun inggih punika wujud enzimipun, jinis iketanipun, interaksi elektrostatik, kaawehan lan panampi proton (ing reaksi asem utawi basa), lan sanèsipun.[41] Reaksi kimia ingkang kalangsungan ing salebeti salira makluk urip limrahipun ugu dipuntepang kaliyan sebatan metabolisme. Ing antawisipun sadaya reaksi-reaksi punika, reaksi ingkang wigatos inggih punika reaksi anabolisme, ing pundhi DNA lan enzim-terkontrol memproses pembentukan protéin lan karbohidrat saking senyawa-senyawa ingkang langkung alit.[42] Bioenergitika nyinaoni sumber ènergi kanggé reaksi biokimia. Sumber ènergi ingkang wigati ing reaksi punika glukosa, ingkang dipunproduksi tuwuhan nglampahi prosès fotosintesis. Sedaya organisme mbetahaken glukosa kanggé memproduksi adenosin trifosfat (ATP), ingkang dipun-ginakaken makhlukurip kanggé njalanaken aktivitaipun.
Penggunaan reaksi kimia
[besut | besut sumber]
Reaksi kimia punika asring dipun-ginakaken déning para ahli tèhnik kimia kanggé mensintesis senyawa énggal saking sumber daya alam mentah ing alam, kados ta lenga bumi lan bijih-bijih mineral. punika ingkang wigati kanggé ndamel reaksi ingkang seefisien, memaksimalkan kasil ingkang saged pikoleh lan meminimalkan reagen ingkang dipunagem, ènergi mlebet lan ènergi medhal. Katalis limrahipun dipun-ginakaken kanggé ngirangi ènergi aktivasi pramila ningkataken laju reaksinipun.[43][44] Pinten-pinten reaksi ingkang spesifik gadhah ngginakaken ingkang mlipun. Tuladhané, reaksi termit dipundamel kanggé ngasilaken surya lan benter ing piroteknik lan pengelasan. Manawi reaksi punika langkung anggel dipunkontrol manawi reakai-reaksi sadèrèngipun, nanging piranti-piranti ingkang dipunbetahaken tebih langkung kedhik lan ngantos punika taksih dipun-ginakaken kanggé ngowahi jalur-jalur kereta api ing panggènan terpelosok.[45]
Ndelengen uga
[besut | besut sumber]- Reaksi organik
- Reaksi kimia anorganik
- Stoikiometri
- Téyori keadaan transisi
- Stoikiometri gas
- Reaksi autokatalitik
- Coefficients
- Q values
- Reaksi endoterm
- Reaksi eksoterm
Cathetan suku
[besut | besut sumber]- ↑ [GoldBookRef|title=chemical reaction|file=C01033 Pengertian Reaksi Kimia](dipununduh Tanggal 30 September 2012)
- ↑ [cite journal|last1=Weyer|first1=Jost|title=Neuere Interpretationsmglichkeiten der Alchemie|volume=7|pages=177|journal=Chemie in unserer Zeit|language=German|year=1973|doi=10.1002/ciuz.19730070604|issue=6 Sajarah Reaksi Kimia] (dipununduh Tanggal 30 September)
- ↑ Leonard J. Friedman & Samantha J. Friedman The History of the Contact Sulfuric Acid Process, Acid Engineering & Consulting, Inc. Boca Raton, Florida] (dipununduh Tanggal 30 September 2012)
- ↑ John E. Lesch The German chemical industry in the twentieth century, Springer, 2000, ISBN 0-7923-6487-2 p. 170 Sajarah Reaksi Kimia]
- ↑ Brock, pp. 34–55
- ↑ Brock, pp. 104–107
- ↑ International Union of Pure and Applied Chemistry. "chemical reaction equation". Compendium of Chemical Terminology Internet edition.
- ↑ Corey, E. J. (1988). "Robert Robinson Lecture. Retrosynthetic thinking?essentials and examples". Chemical Society Reviews. 17: 111. doi:10.1039/CS9881700111.
- ↑ International Union of Pure and Applied Chemistry. "elementary reaction". Compendium of Chemical Terminology Internet edition.
- ↑ Gernot Frenking: Elementarreaktionen. In: Römpp Chemie-Lexikon, Thieme, 2006
- ↑ Atkins, pp. 106–108
- ↑ Wiberg, pp. 810–811
- ↑ Atkins, p. 150
- ↑ a b c To react or not to react? Archived 2010-08-25 at the Wayback Machine.. Utah State Office of Education. Retrieved 4 June 2011.
- ↑ a b Six Types of Chemical Reactions – MrGuch ChemFiesta.
- ↑ Christian B. Anfinsen Advances in protéin chemistry, Academic Press, 1991 ISBN 0-12-034242-1 p. 7
- ↑ A. G. Sykes Advances in Inorganic Chemistry, Volume 36, Academic Press, 1991 ISBN 0-12-023636-2 p. 359
- ↑ Wiberg, pp. 289–290
- ↑ Wiberg, p. 409
- ↑ International Union of Pure and Applied Chemistry. "conjugate acid–base pair". Compendium of Chemical Terminology Internet edition.
- ↑ International Union of Pure and Applied Chemistry. "precipitation". Compendium of Chemical Terminology Internet edition.
- ↑ Jörg Wingender, Stefanie Ortanderl Ausfällung. In: Römpp Chemie-Lexikon., Thieme, July 2009
- ↑ Ralf Alsfasser, Erwin Riedel, C Janiak, HJ Meyer Modern Inorganic Chemistry. 3. Edition. de Gruyter, 2007, ISBN 978-3-11-019060-1, p. 171
- ↑ Atkins, pp. 937–950
- ↑ Christophe Dugave Cis-trans isomerization in biochemistry, Wiley-VCH, 2006 ISBN 3-527-31304-4 p. 56
- ↑ David Stanley Saunders Insect clocks, Elsevier, 2002, ISBN 0-444-50407-9 p. 179
- ↑ International Union of Pure and Applied Chemistry. "catalyst". Compendium of Chemical Terminology Internet edition.
- ↑ International Union of Pure and Applied Chemistry. "inhibitor". Compendium of Chemical Terminology Internet edition.
- ↑ Christoph Elschenbroich: Organometallchemie. 6th edition, Wiesbaden, 2008, ISBN 978-3-8351-0167-8, p. 263
- ↑ Cithakan:JerryMarch
- ↑ S. R. Hartshorn, Aliphatic Nucleophilic Substitution, Cambridge University Press, London, 1973. ISBN 0-521-09801-7 pp. 1 ff
- ↑ Leslie C. Bateman, Mervyn G. Church, Edward D. Hughes, Christopher K. Ingold and Nazeer Ahmed Taher (1940). "188. Mechanism of substitution at a saturated carbon atom. Part XXIII. A kinetic demonstration of the unimolecular solvolysis of alkyl halides. (Section E) a general discussion". Journal of the Chemical Society: 979. doi:10.1039/JR9400000979.
{{cite journal}}: CS1 maint: multiple names: authors list (link) - ↑ Brückner, pp. 63–77
- ↑ Brückner, pp. 203–206
- ↑ Brückner, hal. 192
- ↑ Brückner, hal. 183
- ↑ Brückner, hal. 172
- ↑ Wiberg, pp. 950, 1602
- ↑ International Union of Pure and Applied Chemistry. "Markownikoff rule". Compendium of Chemical Terminology Internet edition.
- ↑ Marye Anne Fox, James K. Whitesell Organic chemistry, 2004, ISBN 0-7637-2197-2 p. 699
- ↑ Peter Karlson, Detlef Doenecke, Jan Koolman, Georg Fuchs, Wolfgang Gerok. Karlson Biochemistry and Pathobiochemistry, 16th edition, Georg Thieme, 2005, ISBN 978-3-13-357815-8, pp. 55–56
- ↑ International Union of Pure and Applied Chemistry. "anabolism". Compendium of Chemical Terminology Internet edition.
- ↑ Gerhard Emig, Elias Klemm. Technical Chemistry. 5th edition, Springer, 2005, ISBN 978-3-540-23452-4, pp. 33–34
- ↑ Trost, B. (1991). "The atom economy—a search for synthetic efficiency". Science. 254 (5037): 1471. doi:10.1126/science.1962206. PMID 1962206.
- ↑ John J. McKetta, Guy E Weismantel Encyclopedia of Chemical Processing and Design: Volume 67 – Water and Wastewater Treatment: Protective Coating Systems to Zeolite, Volume 67[pranala mati permanèn], CRC Press, 1999 ISBN 0-8247-2618-9, p. 109












